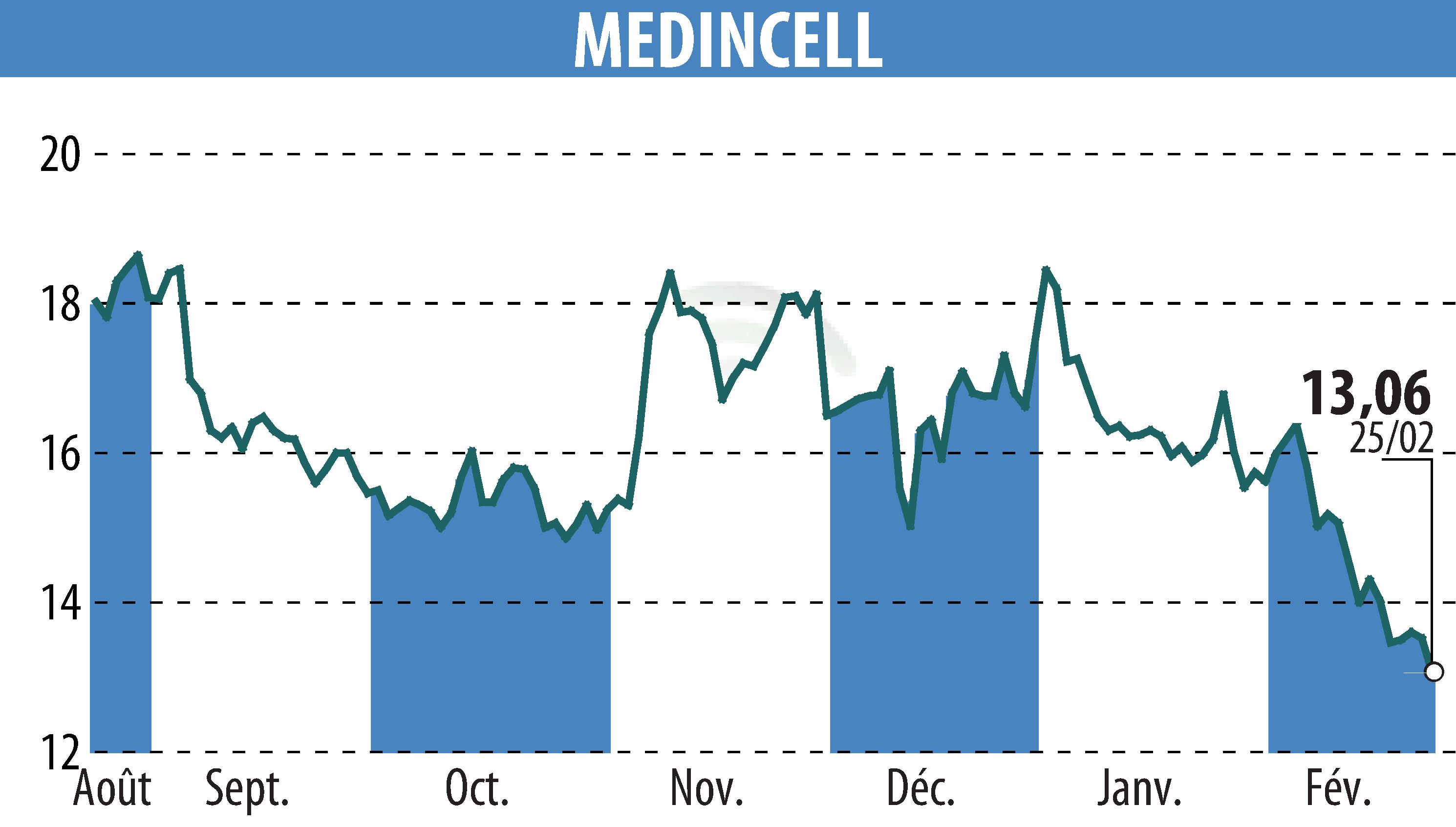
on MEDINCELL (EPA:MEDCL)
La FDA accepte la demande d'utilisation d'UZEDY dans le traitement du trouble bipolaire I
Teva Pharmaceuticals et Medincell ont annoncé que la FDA avait accepté leur demande d'extension de l'indication d'UZEDY®, un antipsychotique injectable, pour inclure le traitement du trouble bipolaire de type I (TB-I). UZEDY est déjà approuvé aux États-Unis pour le traitement de la schizophrénie chez l'adulte par injection mensuelle ou bimensuelle.
La nouvelle demande s'appuie sur les données cliniques existantes de l'UZEDY et sur les conclusions de la FDA concernant les formulations de rispéridone précédemment approuvées pour le traitement de la BP-I. Cette acceptation souligne l'engagement de Teva à faire progresser les traitements en neurosciences.
La forme injectable à action prolongée d'UZEDY répond à des besoins non satisfaits dans le traitement de la BP-I, améliorant potentiellement l'observance du traitement par les patients. Teva supervisera les processus réglementaires et la commercialisation, Medincell étant éligible aux redevances sur les ventes nettes.
R. H.
Copyright © 2025 FinanzWire, all reproduction and representation rights reserved.
Disclaimer: although drawn from the best sources, the information and analyzes disseminated by FinanzWire are provided for informational purposes only and in no way constitute an incentive to take a position on the financial markets.
Click here to consult the press release on which this article is based
See all MEDINCELL news
