on Nanohale AG (isin : DE000A1EWVY8)
Le FYB203 de Formycon reçoit l'approbation réglementaire britannique
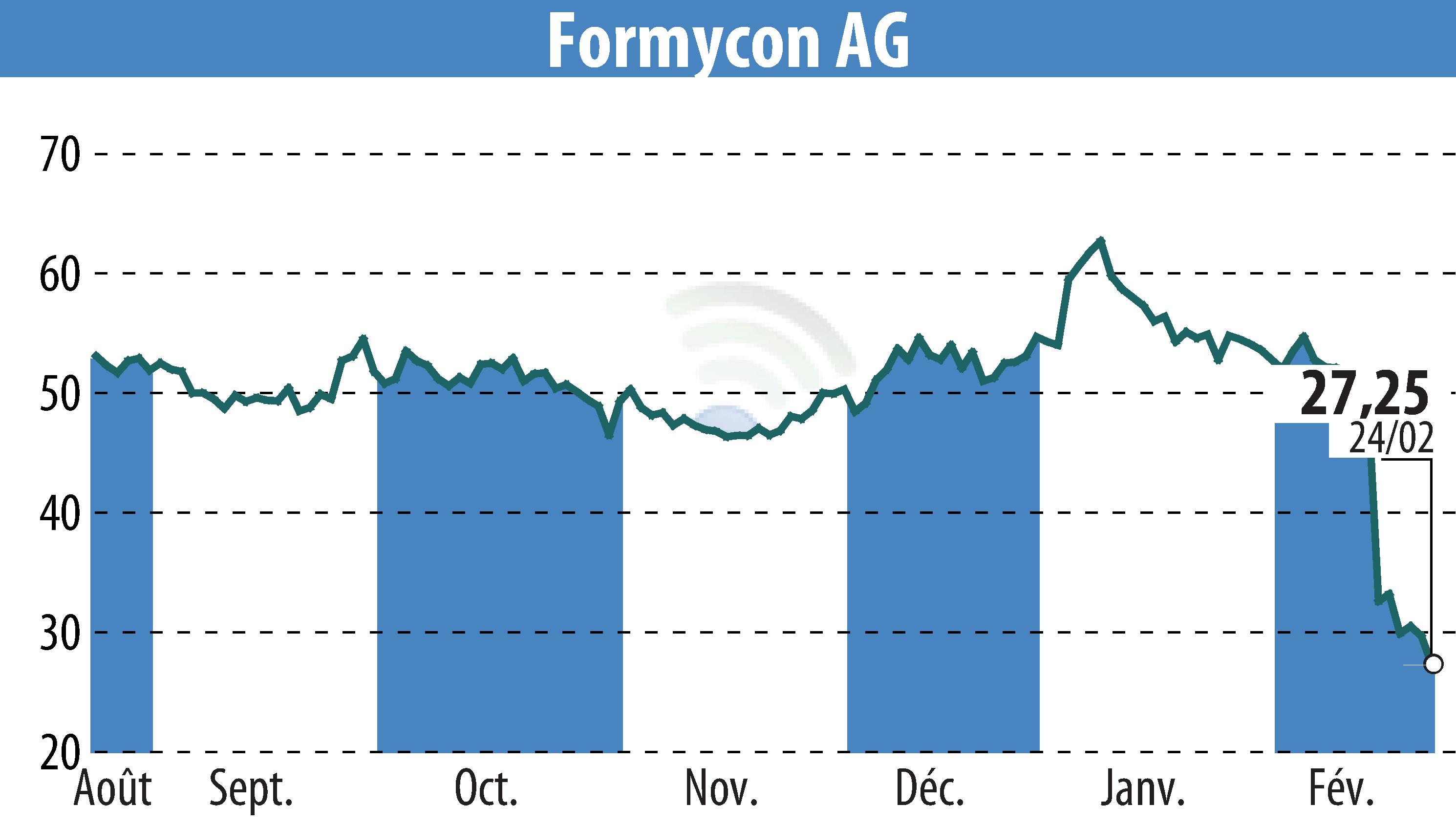
Formycon AG a annoncé que son biosimilaire FYB203 (aflibercept), commercialisé sous la marque AHZANTIVE®, a reçu l'approbation réglementaire au Royaume-Uni. Cette approbation par l'Agence de réglementation des médicaments et des produits de santé (MHRA) permet d'utiliser le FYB203 pour traiter la dégénérescence maculaire néovasculaire liée à l'âge (nDMLA) et d'autres maladies rétiniennes graves.
Cette opération fait suite aux autorisations de mise sur le marché de la FDA américaine et de la Commission européenne. Teva Pharmaceuticals assurera la commercialisation du produit en Europe, y compris au Royaume-Uni. Ce partenariat capitalise sur la présence établie de Teva dans le domaine des traitements ophtalmiques.
Le FYB203 agit comme un inhibiteur du facteur de croissance endothélial vasculaire (VEGF), ciblant la formation anormale de vaisseaux sanguins dans la rétine, responsable des problèmes de vision. Cette autorisation améliore les options pour les patients ayant besoin de traitements rentables pour les affections rétiniennes.
R. E.
Copyright © 2025 FinanzWire, all reproduction and representation rights reserved.
Disclaimer: although drawn from the best sources, the information and analyzes disseminated by FinanzWire are provided for informational purposes only and in no way constitute an incentive to take a position on the financial markets.
Click here to consult the press release on which this article is based
See all Nanohale AG news
