on Monogram Technologies Inc. (NASDAQ:MGRM)
Mises à jour de Monogram Technologies sur la soumission 510(k) après la réunion de la FDA
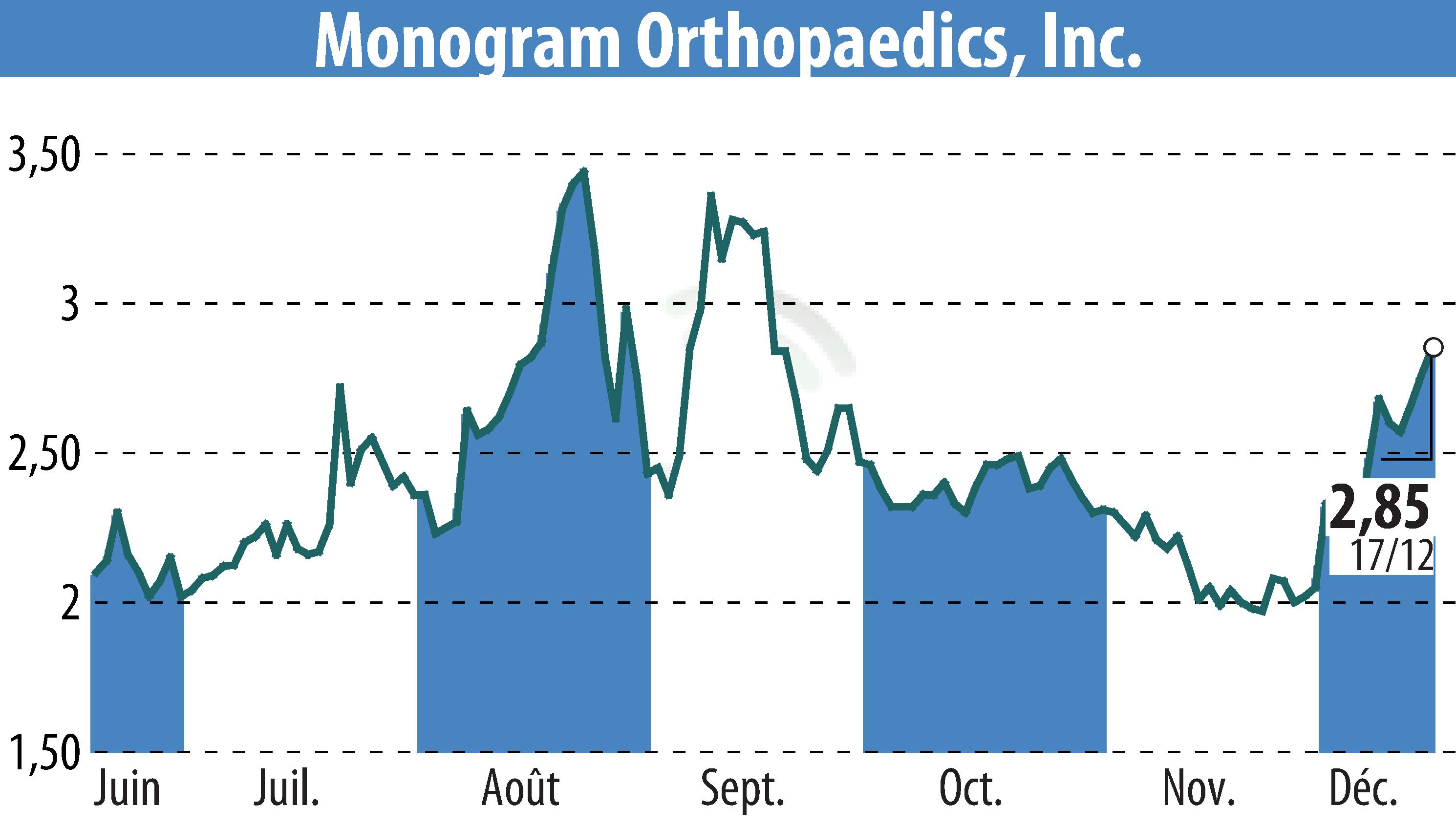
Monogram Technologies Inc., une société de robotique basée sur l'IA, a fait le point sur sa récente réunion avec la FDA concernant la soumission 510(k) pour son système TKA mBôs. Soumise en juillet 2024, la demande a passé l'examen initial mais a été mise en attente dans l'attente d'une réponse complète à la demande d'informations supplémentaires (AIR) reçue en septembre.
Après avoir reçu des réponses écrites et participé à une réunion de demande de soumission le 17 décembre 2024, Monogram estime avoir suffisamment répondu aux préoccupations de la FDA sans avoir besoin de données cliniques. Une réponse complète à l'AIR est prévue au premier trimestre 2025. L'obtention d'une autorisation serait importante pour faire progresser les normes de médecine orthopédique.
La société cherche également à obtenir l'autorisation réglementaire pour les essais cliniques en Inde, avec pour objectif de commencer la formation aux essais d'ici janvier 2025. Le PDG Ben Sexson souligne l'importance stratégique des développements et de la stratégie produit multigénérationnelle.
R. E.
Copyright © 2025 FinanzWire, all reproduction and representation rights reserved.
Disclaimer: although drawn from the best sources, the information and analyzes disseminated by FinanzWire are provided for informational purposes only and in no way constitute an incentive to take a position on the financial markets.
Click here to consult the press release on which this article is based
See all Monogram Technologies Inc. news
